新冠肺炎疫情在全世界持續緊繃,從2019年12月延續到2021年1月,雖然許多疫苗已經逐漸問世,但恐怕也要等到七月以後才會疫情緩和。
同時間,新冠疫情也導致各地的捐血數量急劇下降
美國的血液中心已經發出嚴重短缺的警報,暴露出了當前醫療體系在血液供應來源上的脆弱性。長久以來,科學家們就一直在擔心血液供應的來源會逐漸短缺,其原因不外是以下兩點,第一是靠血液傳播的疾病愈來愈多,造成無法捐血的人也愈來愈多。第二是迅速老年化的人口結構,使得主要捐血來源的年輕人變成少數。這些問題本來就已經在現代社會中逐漸浮現,但沒想到的是,新冠疫情加速了它的到來,因此,研究人造血液的生產方法,更加急迫,期望在捐血來源短缺時,當作天然血液的替代來源,救人無數。
人造血也叫做人工血
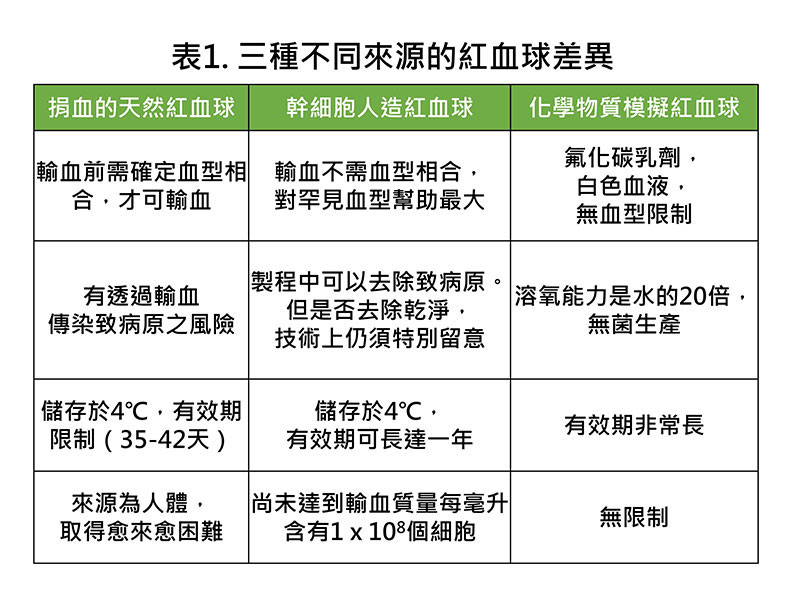
但更為正確的名稱,應該是血液替代品,因為目前不論科學如何進步,都還無法製造出和人類血液完全一模一樣的成分,真正的血液至少包括紅血球、白血球和血小板三種血球,但目前不論是單獨製造紅血球或是血小板,都是超級大工程,更遑論血液中其他成百上千的成分,因此,為因應短時間緊急輸血的需求,只要包含可以攜帶氧氣進來,把二氧化碳帶走的物質,就簡稱為人造血,但其實和真正的血液差距何止十萬八千里,但至少能短暫讓病人獲得足夠氧氣,帶走二氧化碳,繼續生存下去。而目前人造血發展的兩大方向,一個是用身體以外的化學物質來攜帶氧氣,另一個則是使用人類的幹細胞,誘導他們成為紅血球。這幾種來源的血液差別,請詳見表一。
2020年12月10日發表在《幹細胞報告》(Stem Cell Reports)期刊的一項研究中,新加坡科學技術研究局幹細胞生物處理小組主任史蒂夫.吳(Steve Oh)成功的利用幹細胞,在實驗室中製造出比先前含紅血球濃度更高的人造血,向成功製造人造血的方向,又邁出了一大步。
早在2015年,吳主任在實驗室就能利用幹細胞製造出含紅血球的人造血,只是當時的紅血球濃度太低。原因是無法產生出數量多且高質量的未成熟紅血球母細胞(erythroblasts),所以後頭製造出的紅血球數量也跟著受到限制。當時吳主任是使用單層幹細胞來培養,這樣的培養方法限制了細胞的生長數量,這次吳主任改變了生產技術,他利用大型生物反應器來擴增和熟成細胞,於是使得紅血球數量大增,進一步接近人造血液的夢想。
吳主任首先將源自身體上各種組織的多功能幹細胞(iPSCs)附著在俗稱微載體的三度空間支持結構上,然後將它們置於不斷攪拌或搖動的細胞培養器皿中,促進其生長。吳主任解釋說,如此密集生長的細胞培養(並非之前的單層細胞培養),需要大量的生長訊號、養分和氧氣,因此持續攪動的環境才有辦法讓他特調的獨特配方培養液(cocktails)中的許多關鍵成分到達生長的細胞上。吳主任目前擁有這項技術的專利,並且他也是兩家從事幹細胞研究的新加坡生物技術公司Zenzic Labs和SingCell的創始人。該團隊在不同大小的培養平台上重複了此項技術,從裝有5 mL單個孔的平板開始,到500 mL旋轉瓶,足足放大了100倍。
吳主任目前培養出來的紅血球細胞密度可以達到每毫升1.7 x 107個細胞。此外,他們使用來自八個不同來源的多功能幹細胞(像是:臍帶血、骨髓和皮膚等等),都非常成功。吳主任同時使用了一種目前最先進的去核技術,因為紅血球母細胞要變成紅血球,必需要經歷去核作用,即細胞失去細胞核的過程。從多功能幹細胞培養到到成熟的紅血球,整個過程需耗時約35天。
當研究小組將生產出來的紅血球和捐血得來的天然紅血球進行比較時
在攜氧能力方面的差異極小。這篇論文首次證明,我們可以從不同來源的多功能幹細胞開始,在控制懸浮液的環境中,培養並生產出數量龐大的紅血球。荷蘭非營利組織Sanquin裡面,專門研究紅血球生成的科學家Emile van den Akker,在接受美國科學家雜誌訪問時就說到,這是生產人造血液所邁出的一大步,將靜態培養物轉移到可擴充產量的生物反應器中,是本論文最大貢獻的地方。
法國Sorbonne大學教授,同時也是生物技術初創公司Erypharm的總裁杜威(Luc Douay)在接受訪問時也說到,許多團隊一直在尋找利用幹細胞產生紅血球,並最終能用於輸血的方法,其中最大的挑戰仍然是如何擴大生產規模。該公司也正在研究這樣的方法。杜威認為這是一篇有趣的論文,但作者只是放大了實驗室的生產數量,並沒有進一步將它的方法擴大到工廠生產這一個級別。
為了達到輸血在質量上的要求
紅血球數量必須是每毫升含有1 x 108個細胞以上,這個最低標準仍然比起新加坡吳主任團隊目前能夠達到的數量級還要高上10倍,因此新加坡團隊依然沒有到達輸血所需要的水平,只是跨出了一大步。但實驗室所產生的紅血球還是能夠以其他方式先來嘗試使用,例如可以嘗試使用在化療後改善病人副作用,亦或是清除血漿中的毒素,因為這些應用就不需要像輸血一樣,需要那麼高濃度的紅血球細胞,這是最快能夠嘗試使用實驗室人造紅血球產品的方法,但儘管如此,科學家的最終目標仍然是希望能夠應用在輸血上。
(本文作者為陽明大學醫學院藥理學研究所兼任教授)


